科学家揭示OSTα/β蛋白组装与转运新机制
记者从中国科学院物理研究所获悉,由该所科研人员等组成的联合研究团队,成功重构出名为OSTα/β的有机溶质转运蛋白的高分辨率冷冻电镜结构。这一突破首次揭示了该蛋白的新颖组装方式及其转运机制,相关成果于1月29日发表在国际学术期刊《自然》上。
在人体消化脂肪的过程中,OSTα/β功能异常会导致消化不良、胆汁淤积及肝损伤等疾病。尽管OSTα/β在调节激素、应对压力和脂代谢中发挥关键作用,长期以来,科研人员对其组装方式一直不清楚。一个重要原因是缺少对该转运蛋白精细结构和构象变化的直观认识。
OSTα/β蛋白的结构与功能
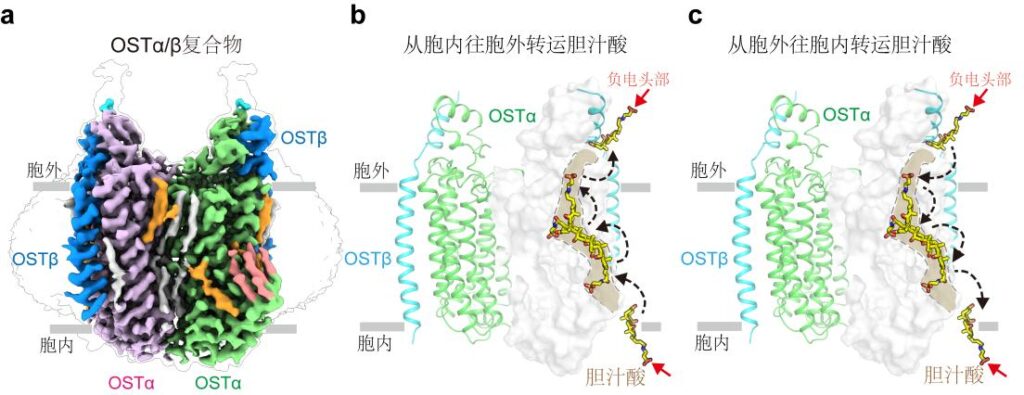
研究发现,OSTα/β由两个OSTα与两个OSTβ亚基组成,各亚基之间的相互作用紧密,保证了OSTα/β的稳定性。此外,研究揭示了OSTα/β中胆汁酸的结合口袋:该口袋内的正电残基与胆汁酸带负电基团相互吸引,从而促进胆汁酸的结合和转运。
研究人员通过分子动力学模拟揭示,胆汁酸在转运过程中会经历一个180度的翻转:胆汁酸头部从朝向细胞内侧翻转到细胞外侧,而OSTα/β结构则保持稳定状态。
“滑梯”模型与传统模型的对比
基于这些结果,研究人员提出了OSTα/β采用新型“滑梯”转运模型。这一模型不同于传统SLC蛋白的“交替访问”转运模型:OSTα/β在底物转运过程中不需要发生大幅度的构象变化,而是利用一个半嵌入膜内的特殊通道,实现胆汁酸从胞内到胞外或者从胞外到胞内的双向转运,转运方向取决于胆汁酸跨细胞膜的浓度梯度。
这一研究解决了长期以来关于OSTα/β组装方式和转运机制不明的根本问题,为理解胆汁酸的跨膜运输提供了全新的结构框架。
科学界的反响与未来研究方向
这一发现引起了科学界的广泛关注。许多专家认为,这项研究不仅为生物化学领域提供了新的视角,也可能为相关疾病的治疗提供新的靶点。
“这项研究为我们理解复杂蛋白质的功能提供了新的思路,”一位未参与研究的生物化学专家表示。
未来,研究团队计划进一步探讨OSTα/β在其他生理过程中可能的功能,并探讨其在药物开发中的潜在应用。
更多精彩资讯请在应用市场下载“极目新闻”客户端,未经授权请勿转载,欢迎提供新闻线索,一经采纳即付报酬。


