FDA授予两款快速诊断试剂盒突破性器械认定应对耐药病原体
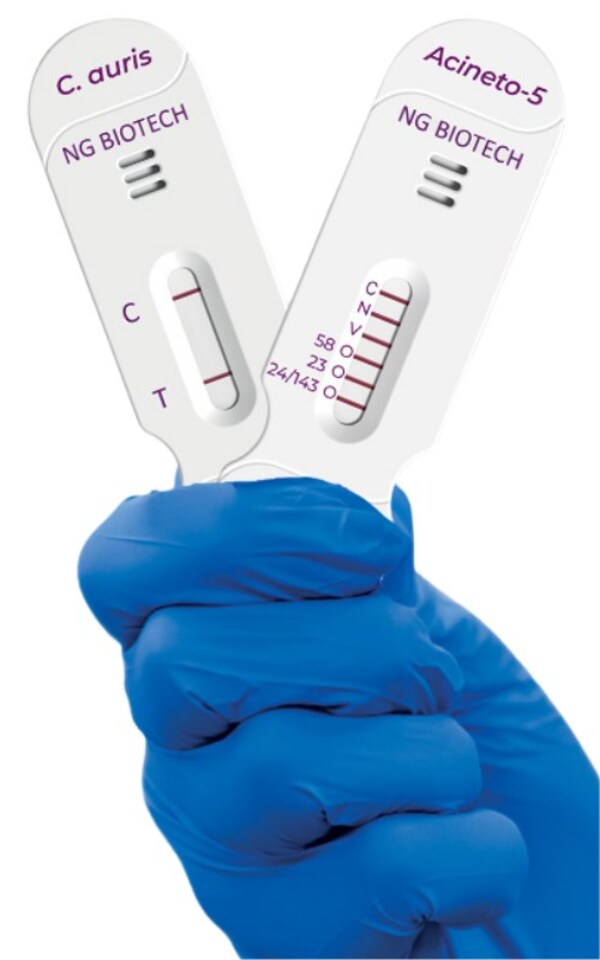
Image of NG-TEST® Candida auris and NG-TEST® Acineto-5® LFA Cassettes
加利福尼亚州圣玛丽亚和法国吉普里——2026年2月19日,美国食品药品监督管理局(FDA)向两款快速诊断试剂盒授予突破性医疗器械认定,标志着抗微生物药物耐药性(AMR)领域的重要进展。这两款试剂盒分别为NG-TEST ® Candida auris 和NG-TEST ® Acineto-5 ®,由NG Biotech与Hardy Diagnostics联合开发,旨在应对危及生命的疾病及未满足的医疗需求。
这两种检测针对的是世界卫生组织(WHO)列为关键优先事项的病原体。Candida auris被列入WHO《真菌重点病原体清单》(2022年),是一种多重耐药酵母菌,已在全球医院引发多起暴发事件。其检测难度大,且死亡率高。与此同时,耐碳青霉烯类鲍曼不动杆菌(CRAB)被列入WHO《细菌重点病原体清单》(2024年),因其耐药谱广且在医疗机构中传播迅速,成为最危险的医院获得性细菌之一。
突破性技术的详细介绍
NG-TEST ® Candida auris是首款专为从培养样本中鉴定Candida auris(耳念珠菌)的快速侧向流免疫测定,可在15分钟内出结果。已发表数据显示,该测定在不同分离株中与参考方法完全一致(100%),支持其在疫情调查和感染控制中的应用。
另一方面,NG-TEST ® Acineto-5 ®可直接从不动杆菌样本中检测并区分五大主要碳青霉烯酶家族——OXA-23类、OXA-24/143类、OXA-58类、VIM及NDM——同样可在15分钟内出具结果。该试剂盒无需PCR,操作简便,无需专用设备。
专家观点与市场影响
NG Biotech首席执行官Milovan Stankov-Pugès表示:“这些突破性认定,既验证了我们试剂盒背后的技术,也肯定了它们所应对的实际需求。”
Hardy Diagnostics首席科学官Andre Hsiung补充道:“此项认定突显了当前对于快速检测医疗机构中构成严重威胁的多重耐药菌的紧迫性与日俱增。”
“通过加快高风险病原体的检测,这些突破性的指定测试旨在加强监测,指导感染控制决策,并支持全球抗击抗菌素耐药性的努力。”
未来的挑战与机遇
该试剂盒由NG Biotech在法国开发和制造,由Hardy Diagnostics在美国独家分销。在FDA继续审查期间,它们目前仅可供研究使用。然而,这一突破为全球医疗机构提供了新的工具,以更快地识别和控制致命的耐药病原体。
随着抗菌素耐药性问题的日益严重,快速、准确的诊断工具变得尤为重要。根据世界卫生组织的数据,抗微生物药物耐药性每年导致全球数十万人死亡,且这一数字预计将继续上升。这一发展不仅为医疗机构提供了新的手段,也为全球公共卫生策略提供了新的方向。
通过这些创新,NG Biotech和Hardy Diagnostics正引领着一场可能改变游戏规则的医疗革命,为全球抗击耐药病原体的斗争提供了新的希望。






